來源:肺癌康復圈KRAS突變號稱史上最難癌基因,但這個在過去讓醫生們束手無策的基因突變,如今涌現出眾多抗癌藥:AMG510、MRTX-849、RMC-4630、PD-1……最強肺癌控制率達100%!40年前,科學家發現了KRAS基因突變可能
來源:肺癌康復圈
KRAS突變號稱史上最難癌基因,但這個在過去讓醫生們束手無策的基因突變,如今涌現出眾多抗癌藥:AMG 510、MRTX-849、RMC-4630、PD-1……最強肺癌控制率達100%!
40年前,科學家發現了KRAS基因突變可能和癌癥發生有關。據統計,大約22%的癌癥患者都有KRAS突變,尤其是胰腺癌(68%)、膽管癌(27%)和肺癌(17%)……
所以,如果有藥物抑制KRAS突變,就能治療這些患者。
曾經,很多藥物都嘗試過去攻克KRAS這個堡壘,司美替尼、卡比替尼、玻瑪西林……但全部失敗了。
因此,很多人認為:KRAS基因沒有成藥性,根本沒有藥物可以降服它。
但近幾年,多個針對KRAS靶點的抑制劑相繼研發,讓KRAS突變“不可成藥”的魔咒將成為歷史。
最不想看到的基因突變—KRAS突變
KRAS屬于RAS基因家族主要成員之一,KRAS基因實際上是人體內的一個正常基因,抽煙、遺傳等很多因素可以引起KRAS基因中堿基配對發生錯誤,出現突變。KRAS基因突變占非小細胞肺癌(NSCLC)總數的20%~30%,肺腺癌較高,肺鱗癌中比較罕見,KRAS G12C是最常見的KRAS突變類型。
醫生和病人最不愿意看到KRAS基因突變,一方面因為KRAS基因突變是影響TKI類靶向藥物療效的不利因素,只要有KRAS基因突變,常見的針對EGFR、ALK、ROS1等基因的靶向藥物都無法使用。另一方面,具有KRAS基因突變的肺癌患者往往化療藥物效果不佳,使用培美曲塞、紫杉醇等一線藥物聯合鉑類化療效果要比沒有KRAS突變的病人要差。
但是,魔高一尺,道高一丈。在科學家持續不斷的努力之下,KRAS這座堡壘終于被轟開了幾個小口。最近幾年,多個靶向或者免疫治療藥物,在KRAS突變患者身上展現了“優秀”的臨床數據,下面就一起來一探究竟。
AMG 510首造奇跡,單藥有效率可達54%
AMG 510是一種新型小分子抑制劑,它可通過對突變KRAS蛋白的12號半胱氨酸(G12C)進行不可逆的結合,而將其鎖定在失活狀態。由于它對KRAS G12C有高度選擇性,因此AMG 510無論是作為單藥,還是與其他靶向療法和免疫療法進行組合,都有望帶來高度的治療潛力。據了解,研發公司通過篩選了六百多個化學分子后,才得到AMG 510這個小分子抑制劑。
AMG 510在去年的ASCO、WCLC和ESMO三大腫瘤會議上亮相。I期研究的結果顯示,AMG 510治療KRAS突變的NSCLC(非小細胞肺癌)患者的總ORR(客觀緩解率)為48%,DCR(疾病控制率)為96%。在13名接受劑量為960 mg AMG 510的NSCLC患者中,ORR為54%,DCR為100%。
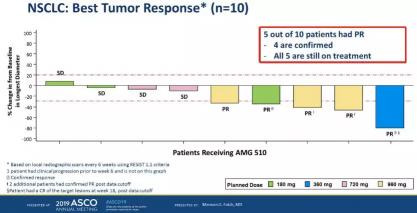
AMG 510是近些年來第一個達到臨床階段的KRAS G12C抑制劑。此外研究還發現AMG 510可以增敏PD-1抗體的療效,國外已經啟動AMG510聯合PD-1的臨床試驗,讓我們拭目以待。
更好的消息是,這款有望攻克KRAS的抗癌新星已經來到中國,即將正式開展臨床試驗。3月9日,CDE(國家藥監局藥品審評中心)官網公布,安進公司研發的KRAS G12C抑制劑AMG 510臨床申請獲藥審中心承辦,意味著將在不久后開始招募國內晚期腫瘤患者,科普君將會密切關注,及時為大家提供招募信息。
MRTX849后線治療KRAS,控制率100%
MRTX849是一款針對KRAS G12C突變開發的特異性小分子口服抑制劑。其對KRAS G12C突變體的抑制效果在納摩爾(nM)水平即可顯現,且具非常好的選擇性,對KRAS G12C的選擇性是野生型KRAS和其它蛋白上胱氨酸的1000倍以上。此外,MRTX849還具有口服利用度高、半衰期長等多個優點。 下面一起來看一下MRTX849的研究時間軸:
2017Mirati披露了KRAS G12C抑制劑的臨床前研究,聲稱計劃下半年獲得IND(新藥臨床試驗)申報的候選化合物;
2018.4Mirati公布化合物代號為MRTX-849;
2018.10Mirati遞交IND(新藥臨床試驗)申請,30天后獲FDA批準;
2019.1MRTX849的I期臨床開展;
2019.10MRTX849的I期/II期臨床試驗數據公布。
一期臨床研究納入了17例既往接受過全身治療的KRAS G12C突變晚期實體瘤患者,12例患者可供評估(6例NSCLC,4例結直腸癌,2例闌尾癌),而最終的實驗數據也是相當完美。
在經過治療后,6例肺癌患者,3例腫瘤明顯縮小,3例病人疾病穩定。12例療效可評價的患者,抗癌控制率高達100%,肺癌客觀有效率為50%。
入組的患者,絕大多數都是至少接受過3種以上不同標準治療方案失敗的難治性晚期癌癥病友,入組該臨床試驗后,依然取得了100%的腫瘤控制,的確是潛在的重磅炸彈級的靶向藥。
其中一個典型的病歷就是一名61歲的晚期肺癌患者,接受過6種方案的化療、1種MEK抑制劑靶向治療、1種PD-1抗體治療(K藥),均失敗——6種化療、1種靶向藥、1種免疫治療,均失敗的晚期肺癌,不得不說是極端難治的“無藥可救”的狀態,而入組臨床試驗后,腫瘤縮小62%,且療效一直保持。
RMC-4630后線控制率67%,聯合AMG 510開啟新試驗,直奔KRAS雙靶治療時代!
RMC-4630是口服的SHP2變構抑制劑,臨床前研究顯示,RMC-4630對于SHP2依賴型RAS信號突變有抑制作用,如KRAS G12C、NF1、BRAF、KRAS擴增等等。這是繼去年AMG 510及MRTX849兩藥問世后,第三個備受矚目的KRAS藥物。
該藥的臨床試驗前期數據共分析了18例KRAS突變晚期NSCLC患者的療效。結果顯示,最佳療效DCR為67%。對于KRAS G12C突變患者,DCR達到75%。有望和AMG 510及MRTX849組成治療KRAS的三叉戟。
值得鼓舞的是,細胞學研究顯示AMG 510與SHP2抑制劑聯合治療KRAS G12C腫瘤有不錯的協同作用,療效優于其他組合。因此,科學家們已經準備RMC-4630與AMG 510聯合用藥,開啟KRAS突變雙靶治療的臨床試驗探索。
KRAS突變更容易從PD-1治療中獲益,免疫治療不缺席
免疫治療作為近些年發展的大趨勢,對于KRAS突變患者的治療同樣值得關注。研究發現KRAS突變患者的PD-L1表達和TMB(腫瘤突變負荷)更高。PD-L1表達和TMB越高,通常免疫治療效果越好。
而且在2019年底的ESMO免疫腫瘤學大會上報道了K藥(帕博利珠單抗)的兩個探索性分析,結果顯示:K藥單藥或聯合化療一線(初始)治療KRAS突變非鱗非小細胞肺癌療效良好,客觀緩解率40%以上。K藥單藥治療KRAS突變,PD-L1陽性患者,客觀緩解率達到56.7%。可見,免疫治療在KRAS突變患者中可能會取得意想不到的效果。
針對EGFR和BRAF等其他驅動癌癥發展的突變,研究人員們已經成功開發了個體化的療法。而作為史上最難攻破的基因突變KRAS,相信也會很快趕上其他突變基因的步伐,研制出可以臨床應用的靶向藥。而我們患者在病理確診后,首先必須要做的事情是:基因檢測,基因檢測,基因檢測,重要的事情說三遍!根據檢測結果找到最適合我們的治療方法。我們也期待新藥早日上市,造福大眾!
參考來源:
[1] Theclinical KRAS(G12C) inhibitor AMG 510 drives anti-tumour immunity. https://doi.org/10.1038/s41586-019-1694-1
[2]Jude Canon et al. The clinical KRAS(G12C) inhibitor AMG 510 drives anti-tumour immunity. Nature(2019).
[3]TheKRASG12C Inhibitor, MRTX849, Provides Insight Toward Therapeutic Susceptibilityof KRAS Mutant Cancers in Mouse Models and Patients.CancerDiscov. 2019 Oct 28. pii: CD-19-1167. doi: 10.1158/2159-8290.CD-19-1167
[4]Borghaei, H., et al.,Nivolumab versus Docetaxel in Advanced Nonsquamous Non-Small-Cell Lung Cancer.N Engl J Med, 2015. 373(17): p. 1627-39.
[5]Chengming Liu et al. The superior efficacy of anti-PD-1/PD-L1 immunotherapy in KRAS-mutant nonsmall cell lung cancer that correlates with an inflammatory phenotype and increasedimmunogenicity.2019
[6]Eric Tran, et al.,T-Cell Transfer Therapy Targeting Mutant KRAS in Cancer . N Engl J Med2016;375:2255-62.
#醫師報超能團#
#超能健康團#

