學習目標:
1��、掌握實驗室制取氧氣的原理、裝置和操作;
2、認識催化劑和催化反應��;
3�����、認識分解反應��。
一、加熱高錳酸鉀(或加熱氯酸鉀)制取氧氣

實驗裝置
(一)實驗藥品
高錳酸鉀:暗紫色固體。(或氯酸鉀:白色固體��,二氧化錳:黑色固體)
(二)實驗原理(以加熱高錳酸鉀為例)
高錳酸鉀在加熱的條件下生成錳酸鉀�����、二氧化錳和氧氣��。

高錳酸鉀制取氧氣的化學方程式
(三)實驗裝置
選擇的儀器:酒精燈、試管�����、鐵架臺(帶鐵夾)��、導管�����、單孔橡膠塞、集氣瓶����、水槽����。
1����、發生裝置
選擇的依據是反應物的狀態和反應條件�����。由于高錳酸鉀是固體�����,反應條件需要加熱,因此選擇:“固體加熱型”發生裝置��。
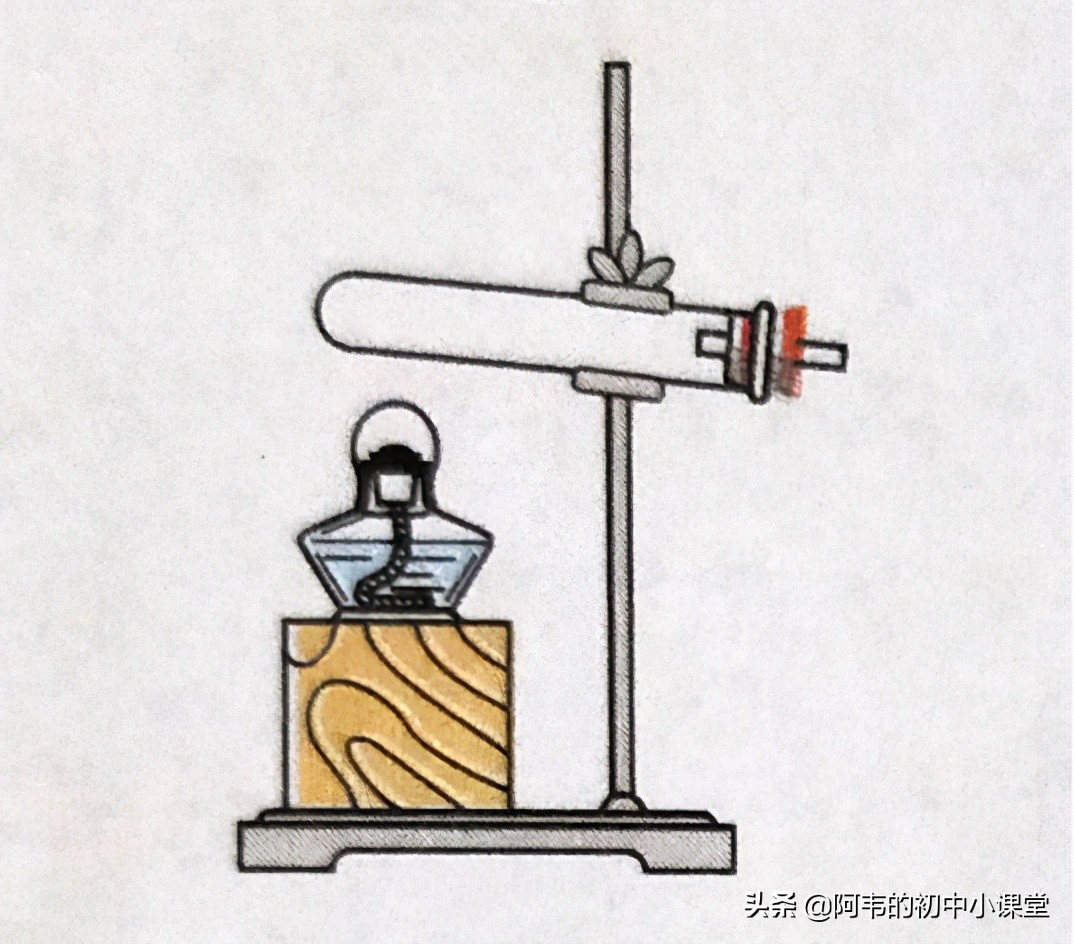
固體加熱型-發生裝置
該裝置需要注意以下要點:
①試管口要略向下傾斜�����;
②鐵架臺的鐵夾要夾在試管的中上部或距離試管口1/3處����;
③伸入試管內的導管不宜過長�����;
④先使試管均勻受熱再集中加熱藥品部分����;
⑤加熱高錳酸鉀制取氧氣時�����,試管口要放一團小棉花����。
2�����、收集裝置
從氣體的溶解性和氣體的密度兩方面考慮(根據氧氣的物理性質)����。
①排水法(原因:氧氣不易溶于水)
注意:導管不能伸入集氣瓶過長��,防止取出集氣瓶時漏氣�����。收集到的氣體較純凈。
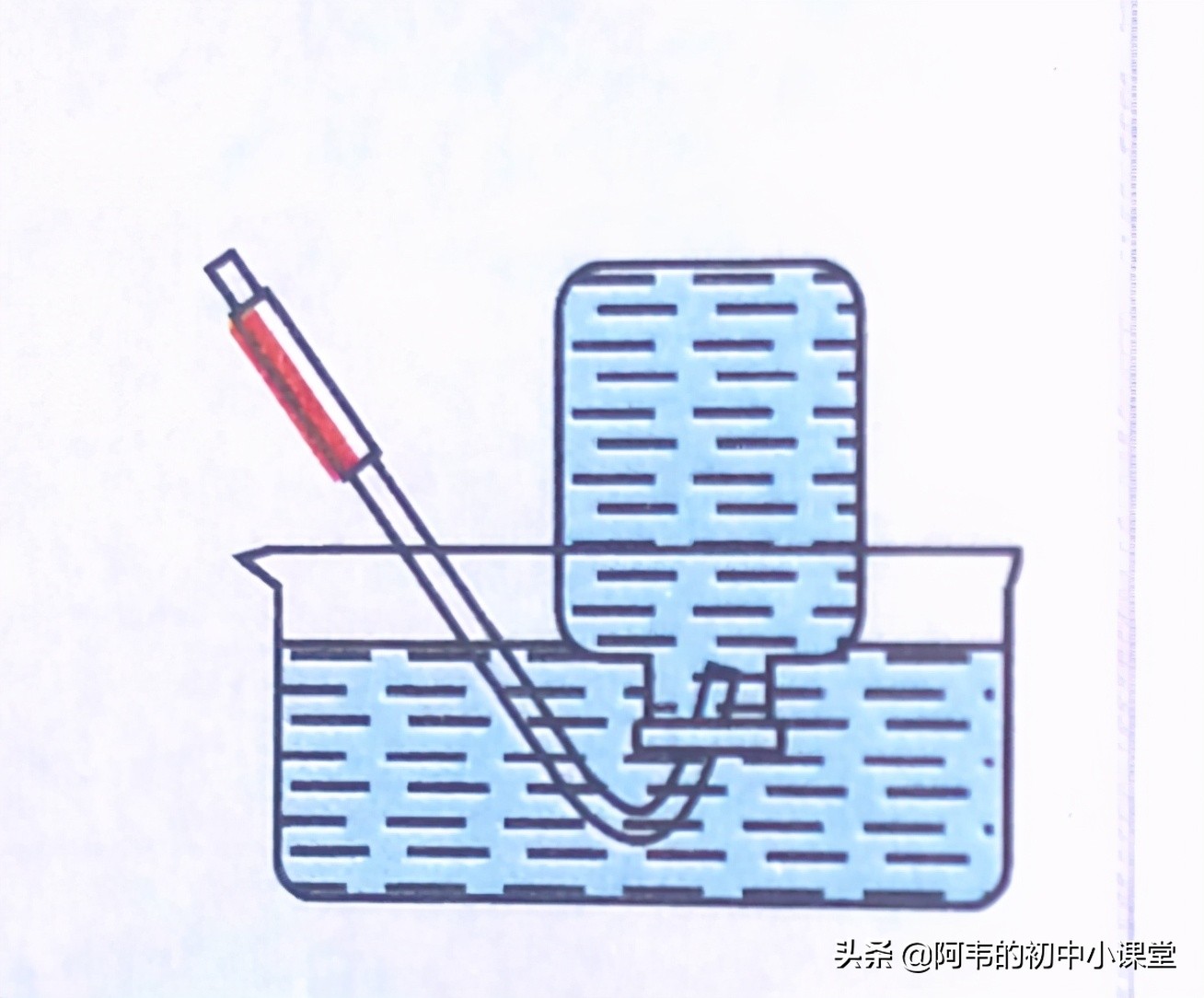
排水法收集氧氣
②向上排空氣法(原因:氧氣的密度略大于空氣)
注意:導管下端必須接近集氣瓶底部����,有利于瓶中空氣的導出��。收集到的氣體較干燥。

向上排空氣法收集氧氣
(四)實驗步驟
1��、檢查裝置的氣密性
方法:先將導管的一端放入水中�����,用手緊握試管外壁��,若水中導管口有氣泡冒出,松開手����,過一會兒,導管內形成一段水柱,則說明裝置氣密性良好����。
2����、裝藥品
先將高錳酸鉀裝入試管底部��,然后在試管口處塞一團棉花�����,并用帶有導管的橡膠塞塞緊試管。
3�����、固定裝置
將試管口略向下傾斜固定在鐵架臺上��。
4�����、點燃酒精燈
點燃酒精燈,并用酒精燈外焰在試管下方來回移動,讓試管受熱均勻����,然后對準試管中的藥品部位集中加熱�����。
5、收集氣體
用排水法收集。
注意以下幾點:
①集氣瓶必須裝滿水�����;
②當導管口有連續均勻的氣泡冒出時再開始收集��,否則收集的氧氣會混有空氣����,導致收集到的氧氣不夠純凈�����。
當收集滿一瓶氣體后����,我們在水下蓋好玻璃片��,然后取出集氣瓶正放在桌面上����。
取出集氣瓶正放在桌面上
6�����、撤離導管
收集氧氣結束后����,將導管撤離水槽��。
7����、熄滅酒精燈
當導管移出水槽后�����,用燈帽蓋滅酒精燈。
【補充】
加熱氯酸鉀制取氧氣
實驗原理如下:
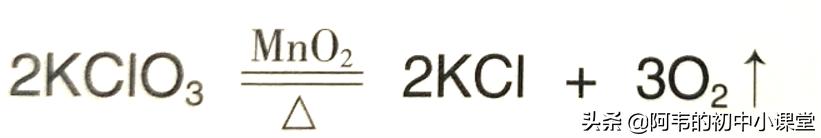
氯酸鉀制取氧氣的化學方程式
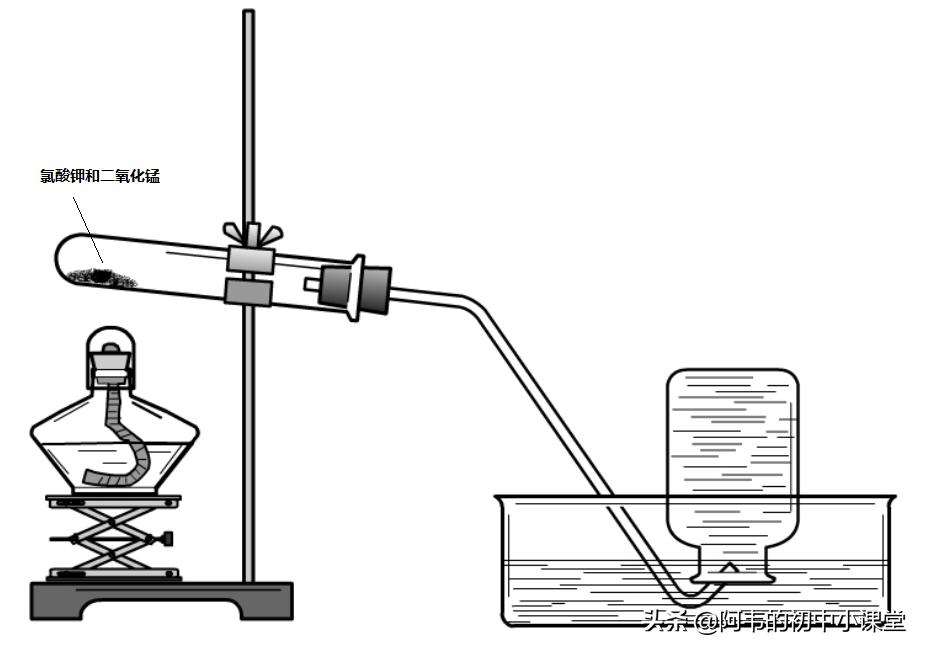
氯酸鉀制取氧氣的實驗裝置
二��、用過氧化氫制取氧氣

過氧化氫制取氧氣的實驗裝置
(一)實驗藥品
過氧化氫�����,俗稱雙氧水��,無色溶液;
二氧化錳�����,黑色固體����。
二、實驗原理
過氧化氫在二氧化錳的催化作用下生成水和氧氣����。

過氧化氫制取氧氣的化學方程式
(三)實驗裝置
選擇的儀器:長頸漏斗��、錐形瓶、導管��、雙孔橡膠塞����、集氣瓶。
1�����、發生裝置
選擇的依據是反應物的狀態和反應條件����。由于過氧化氫是液體�����,二氧化錳是固體��,反應條件不需要加熱��,因此選擇:“固液常溫型”發生裝置。
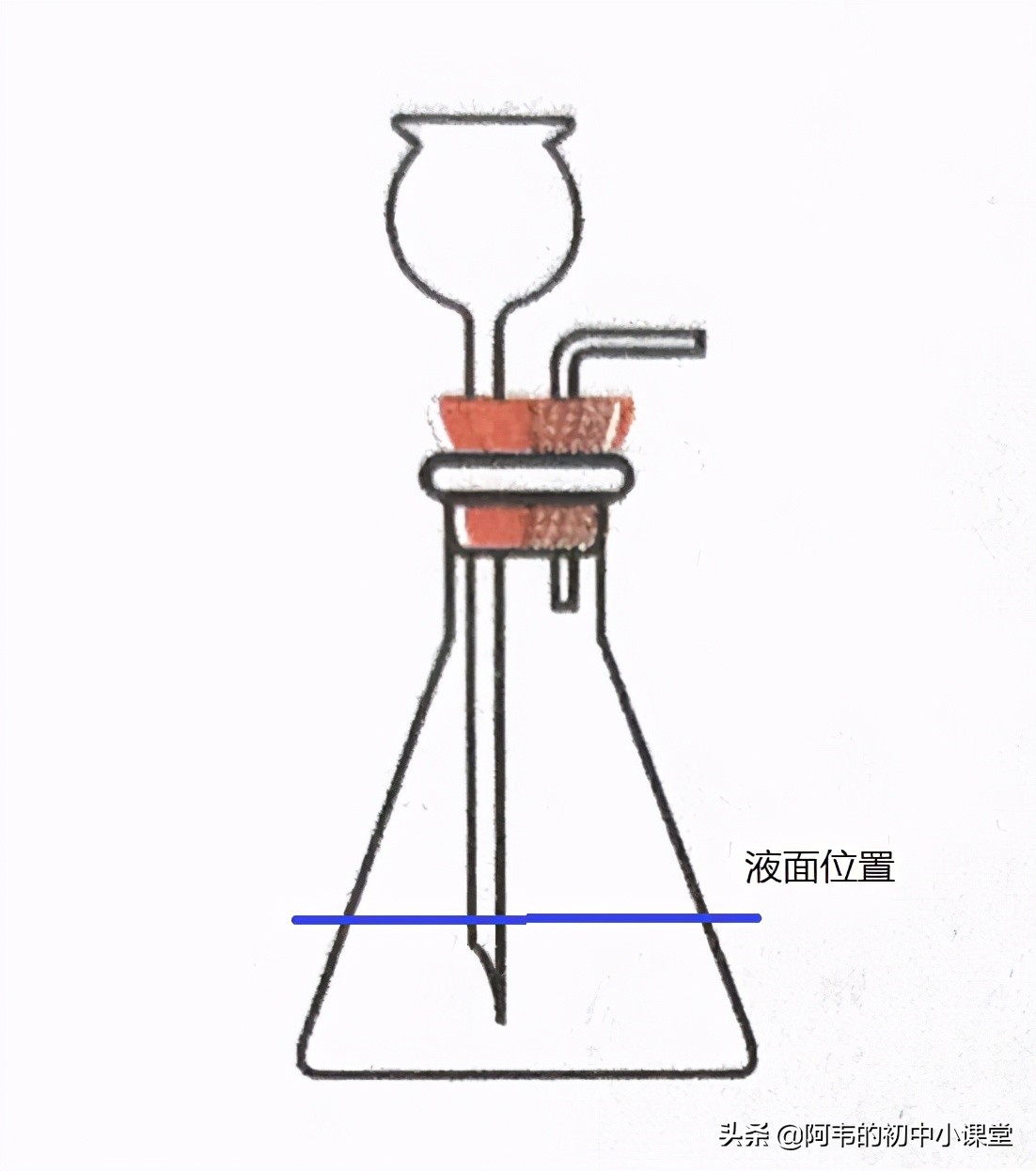
固液常溫型-發生裝置
注意:長頸漏斗末端應在液面以下��,防止氧氣從長頸漏斗中逸出�����。
2����、收集裝置(參考“加熱高錳酸鉀制取氧氣”)
(四)實驗步驟
1�����、檢查裝置的氣密性
方法:先往長頸漏斗中注入水直至長頸漏斗末端在液面以下��,關閉彈簧夾,繼續向長頸漏斗中注入水����,若觀察到長頸漏斗內的液面不下降��,則說明裝置氣密性良好。
2、裝藥品
先向錐形瓶加入二氧化錳固體�����,然后塞好帶有長頸漏斗和導管的雙孔橡膠塞�����,再向長頸漏斗中加入過氧化氫溶液。
3�����、收集氣體
用向上排空氣法收集��。
注意以下幾點:
①導管下端必須接近集氣瓶底部����,有利于瓶中空氣的導出��;
②當收集滿一瓶氣體后��,先移出導管,再蓋好玻璃片,注意集氣瓶應正放在桌面上。
氧氣驗滿的方法:將帶火星的木條放到集氣瓶口�����,若木條復燃�����,則證明已收集滿��。
三、催化劑和催化作用
(一)概念
1����、催化劑
在化學反應里能改變其他物質的化學反應速率,而本身的質量和化學性質在反應前后都沒有發生變化的物質叫作催化劑(又叫觸媒)����。
2��、催化作用
催化劑在化學反應中所起的作用叫作催化作用。
(二)催化劑的特點
1��、一變:改變化學反應速率����,包括加快和減慢。
2��、二不變:反應前后催化劑本身質量不變����,化學性質不變�����。
(三)催化劑的作用
生產化肥,農藥����,化工原料等����。
四��、分解反應
1�����、概念:由一種反應物生成兩種或兩種以上其他物質的反應,是化學反應的基本類型��。
2�����、特點:一變多。

