這座異軍突起的金礦究竟好不好挖?來源:甲子光年作者:芊乂編輯:火柴Q核心要點:·疫情蔓延全球,中國IVD(體外檢測)行業出海量激增后又遇挫。·目前針對新冠病毒的檢測方法主要是分子診斷和免疫診斷,準確性是共同難點。·高門檻、高毛利的全球IVD
這座異軍突起的金礦究竟好不好挖?
來源:甲子光年
作者:芊乂 編輯:火柴Q

核心要點:
· 疫情蔓延全球,中國IVD(體外檢測)行業出海量激增后又遇挫。
· 目前針對新冠病毒的檢測方法主要是分子診斷和免疫診斷,準確性是共同難點。
· 高門檻、高毛利的全球IVD市場高度集中于5大跨國公司,中國IVD正在逐步實現國產化替代,但關鍵材料和設備仍被卡脖子。
· 此次疫情,讓中國IVD行業的窗口期和洗牌期一起到來。
“我們3月17號剛剛通過歐盟CE認證,18號就接到了最少50萬份的海外訂單。”自研新冠病毒體外檢測試劑盒獲得歐盟準入許可的消息剛發布,海普洛斯CEO許明炎就在蜂擁而至的十幾家代理經銷商中挑花了眼。接受采訪的當日下午,他剛跟兩家經銷商敲定了合作關系。
截至目前,國家藥監局共審批通過17家企業的19個新冠病毒檢測試劑產品,其中,核酸檢測試劑11個,抗體檢測試劑8個。
與國內的謹慎節制相比,國產試劑盒的出海之路可謂暢通無阻。
進入3月以來,已有80多家國產新冠病毒試劑盒廠商通過了歐盟CE認證,這表明它們生產的產品達到了歐盟醫療器械相關指令的符合性要求,不僅可在歐洲經濟區(27個歐盟成員國以及冰島、列支敦士登和挪威)銷售,還可在歐洲經濟區以外,雖沒有簽署相互承認協議(MRA)但認可CE標志的國家銷售。
這些企業中,有不少科創板熟面孔,如達安基因、萬孚生物、美康生物、凱普生物、華大基因、三諾生物、邁克生物等;也有處于成長期的后起之秀,如海普洛斯、銳翌生物、真邁生物、博奧賽斯等。
它們都屬于體外診斷,即IVD(In Vitro Diagnosis)行業,即在人體之外,通過對血液、體液、組織等人體樣品進行檢測而獲取臨床診斷信息的產品和服務,主要由診斷設備和診斷試劑構成。
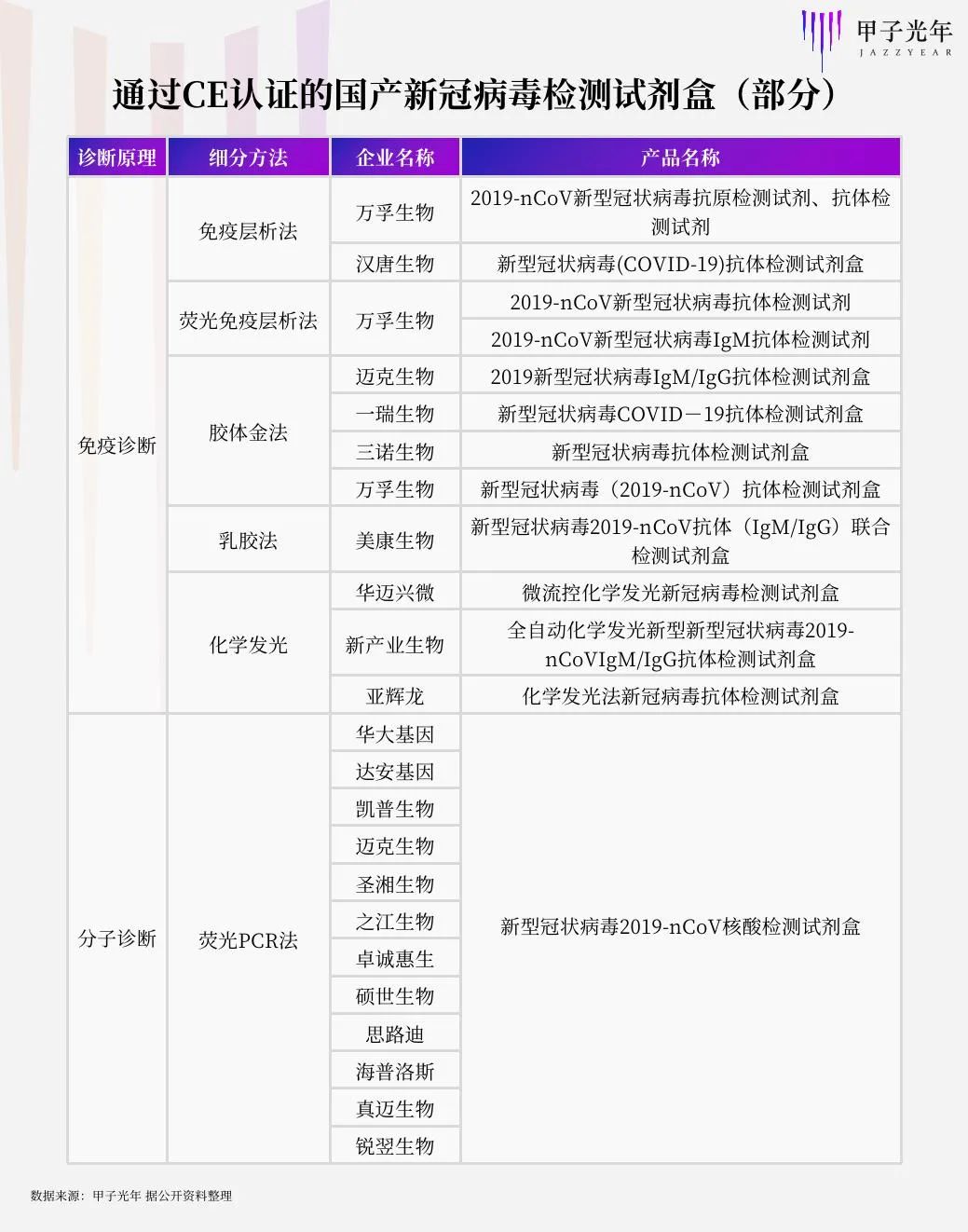
隨著新冠疫情蔓延全球,中國IVD行業似乎迎來了前所未有的出海契機。
在此之前,除了有潛力彎道超車的基因測序方法,國內IVD廠商一直處于跟仿歐美技術的早期發展階段。
而好消息還沒持續太久,卻出現了令人尷尬的一幕:
3月下旬以來,西班牙、荷蘭、波蘭等國聲稱由于準確率等產品質量問題,將不再進口包括試劑盒、口罩和呼吸機在內的中國醫療產品。
中國商務部也拔高了國貨的出海門檻,“現在沒有拿到國內資質的新冠檢測試劑盒已經禁止出口了。”許明炎告訴「甲子光年」。
暴增的海外訂單,注定是一錘子買賣嗎?被高毛利誘惑入局的新企業是能長久促進行業發展還是帶起泡沫?
本文,「甲子光年」采訪了包括華大因源(華大基因下屬子公司)、海普洛斯、真邁生物等在內的國內多家IVD企業,以及遠毅資本、華夏基石等大健康領域的第三方投資、研究機構,來聊聊這座異軍突起的金礦究竟好不好挖。
1.國產試劑盒,墻里開花墻外香
2月22日是一個全球的疫情轉折點,這一天,中國21省區市確診病例0新增。而海外疫情卻愈演愈烈——當天,全球除中國外確診病例已逾千例,韓國政府把新冠疫情預警上調至最高級別;伊朗組建國家疫情防控部門,關閉了德黑蘭等14個省份的學校;意大利叫停威尼斯狂歡節......
疫情主戰場逐漸開始從中國轉移到海外。
截至4月2日早上7:30,最新全球累計病例已達93萬,其中海外占比達91%。
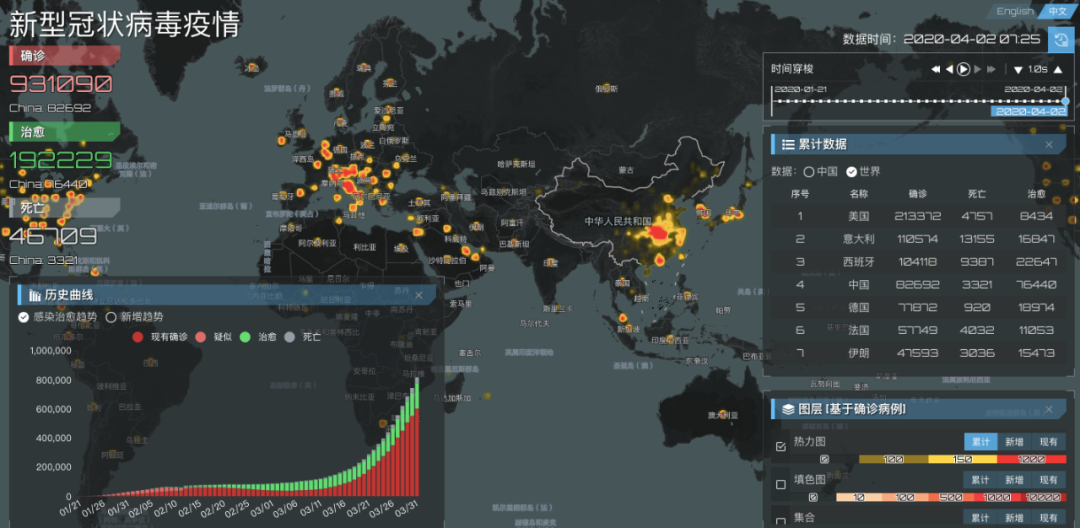
突如其來的疫情,讓意大利、美國、伊朗和西班牙等國家出現了較大的病毒檢測能力缺口。
以西班牙為例,《先鋒報》3月21日報道,西班牙計劃購買600萬個新冠病毒快速檢測試劑盒,4天后還宣布將花費4.32億歐元向中國購買醫療物資,其中包括550萬份核酸檢測試劑盒。
據華夏基石醫療合伙人艾中估計,4月底之前,新冠病毒體外檢測試劑盒將在全球范圍內供不應求。
在此背景下,接二連三獲得歐盟CE認證的國產新冠病毒試劑盒成為了海外市場的香餑餑。
處于行業領軍地位的上市公司動作最快。
1月26日,國家藥品監督管理局(下文簡稱國家藥監局)就應急審批,通過了上海捷諾生物、上海之江生物和華大集團旗下的華大生物與華大智造4家企業的新型冠狀病毒檢測產品。
成長期公司也不甘示弱。
海普洛斯許明炎稱,從大年初一開始,公司臨時組建了一支不到二十人的研發團隊,并在不到一周的時間內,完成了研發制造過程,且在不進行產能擴增的情況下,也能保證每日最低5萬份的產出,之前營收占比僅10%的海外業務,有望在此次疫情中飛速成長為新的增長點。
之所以行動迅速、蜂擁而上,在于IVD,這個對普通人來說比較生僻的行業其實非常賺錢。
由于行業準入門檻相對較高,競品較少,IVD企業的議價能力普遍較強。近年來,伴隨產品升級,國內IVD行業的毛利率穩步上升,在2018年達到了47.29%。
華夏基石艾中告訴「甲子光年」,以IVD中的分子診斷賽道為例,國內企業的毛利甚至高達70%~90%,“這也解釋了一些營收一兩個億的IVD企業能夠上市的原因,他們的利潤可能有三四千萬之多。”
以這次疫情期間出口的核酸檢測試劑盒為例,一份核酸檢測試劑盒的售價約100元人民幣,取毛利率為40%,據多位業內人士提供的數據,目前國內IVD廠商收到的訂單量級在10~100萬份不等,如果經銷商按時、按量提貨,那么一份訂單就可以帶來1000萬~1億人民幣的營收和400~4000萬元的毛利。
第一時間成功研發新冠病毒核酸檢測試劑盒的華大因源(華大基因下屬子公司),在短短一個月內就將海外市場的輻射范圍從30個國家和地區擴大到70個。
其市場部負責人孫經夢告訴「甲子光年」,截至3月22日,華大檢測試劑盒的國際訂貨量就已達百萬人份(人份,復合量詞,以檢測一個標本需要的量為一人份)。3月27日,旗下新型冠狀病毒核酸檢測試劑盒(熒光PCR法)更成為國內首個獲得美國FDA(Food and Drug Administration,食品藥品監督管理局)緊急使用授權(Emergency Use Authorization)的自研產品。
除了被外貿代理商狂轟濫炸的國產IVD研發制造企業,上游供應商和下游貿易平臺也跟著一同火熱 。
如真邁生物是一家IVD上游的設備、試劑生產商,此次也研發出了核酸檢測試劑盒,該產品在獲得CE認證后,已接到4家國內代理的合作需求,并與其中一家達成了正式協議——“他們對PCR熒光檢測試劑盒的需求量都在20萬~50萬人份”,真邁生物CEO顏欽告訴「甲子光年」,此次銷往海外的產品,將覆蓋意大利、伊朗、吉爾吉斯及奧地利,“其實也不限于這些國家,只要符合政策法規,我們都歡迎。”
專注于醫療器械領域供應鏈B2B電商平臺的貝登也借勢開辟了很多新的海外渠道。遠毅資本合伙人楊瑞榮告訴「甲子光年」,僅通過朋友圈的傳播,貝登已接到了來自巴西、阿聯酋、西班牙和瑞士的訂單。
目前,中國IVD廠商斬獲CE認證和海外訂單的消息依然在陸續傳出,其背后的深層原因在于,新冠病毒試劑盒的研發制造并無太多技術壁壘。
從IVD領域各項細分技術在我國的生命周期來看,目前免疫診斷法已較為成熟,分子診斷法的研發、應用進入成長期,國產IVD產品正逐步向靈敏度高、特異性強、檢測速度快和低成本的方向發展。尤其2010年以來,隨著一批基因檢測公司的成立,賽道進入了國產化替代的新階段。
值得注意的是,針對新冠肺炎的IVD產品一度出現了墻里開花墻外香的現象。
一方面,國內審批在收緊。
“現在國內疫情基本控制住了,我們拿不到陽性樣本,所以在國內很難做相關認證。”由于錯失了申報的時機和條件,海普洛斯CEO許明炎表示,公司的產品暫時無法在國內流通,之前的出海市場也限于英國、德國、意大利等歐洲地區。
楊瑞榮向「甲子光年」解釋,在國內最先通過緊急審批的這四家公司,先前都與中國疾控中心(CDC)有合作關系,審批快是因為信任度高。而目前國內需求已基本滿足,審批也恢復了正常節奏,因此在一些IVD廠商看來,會覺得“審批”變難了。
另一方面,一些急缺IVD的地區則在此前一段時間放寬了要求。因此,目前有人質疑不需要臨床認證的歐盟CE標準實際獲批門檻不高,并不能說明通過認證的公司就一定實力過硬。
華夏基石艾中告訴「甲子光年」,疫情之下,措手不及的歐洲各國政府確實放寬了CE認證、ISO13485(醫療器械質量管理體系用于法規的要求)認證,只需提交自我聲明即可,不強制要求審批檢驗記錄,這導致了出口的國貨參差不齊。
海外的寬松政策,為提前投入了相關研發的國內IVD廠商大開方便之門:產品出海,渠道擴增,營收猛漲,一切似乎水到渠成。
不過不少從業者判斷,出海的機會雖然是真的,但這樣的熱鬧勢必回落。
從目前的發展形勢看,回落已經發生,而且是戲劇性的反轉。
2.出海熱的冷思考
令很多短時間內積極投入試劑生產的中國公司錯愕的是,目前海外對中國醫療產品負評如潮,已直接影響到了他們的生意,甚至上升到了外交層面。
3月31日,商務部會同海關總署、藥監局發布了關于有序開展醫療物資出口的公告,要求出口的相關醫療物資必須提供書面或電子聲明,承諾出口產品已取得我國醫療器械產品注冊證書,并符合進口國(地區)的質量標準要求。
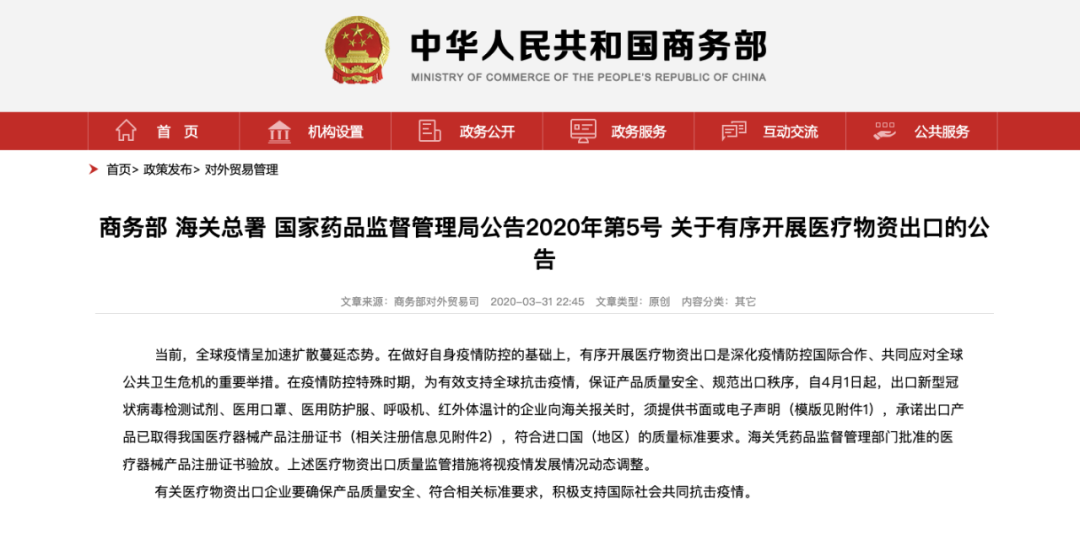
這一波退貨潮的苗頭最初出現在西班牙。
據外媒報道,西班牙多個大型醫院的微生物實驗室使用國產新冠病毒快檢試劑后,認為效果不如預期。西班牙衛生部也于3月26日宣布,計劃退還自中國進口的9000個快速檢測試劑盒。
相關生產商易瑞生物解釋道,操作不當會降低準確度,但這一事件也從側面說明部分通過CE認證的國貨可能存在質控問題。
隨著全球抗疫變得白熱化,國產的新冠病毒檢測試劑盒也被爆出越來越多的假陰、假陽檢測案例。雖然市面上流通的產品,都會聲明90%~95%的準確率,但臨床實踐的情況卻不盡如人意,特殊情況下申請應急審批的產品量大,難免有人魚目混珠。
而客觀來說,國產IVD公司的試劑盒確實也面臨著兩大難題:準確性和量產能力。
具體來看,此次針對新冠病毒研發的國產試劑盒,主要采用了分子診斷和免疫診斷的方法,即熒光PCR(聚合酶鏈式反應)核酸檢測試劑盒與膠體金法抗體檢測試劑盒,前者檢測核酸,后者檢測抗體。
兩種方式都可以進行新冠病毒檢測,區別在于檢測周期和準確性。
核酸檢測試劑盒的周期更短,可以更早發現新冠病毒感染患者。
理論上,感染后1~2天即可檢測到核酸。
而檢測抗體的膠體金法比較滯后——感染一周左右才可檢測到IgM抗體,感染兩周左右可檢測到IgG抗體。
準確性上,也是核酸檢測優于膠體金法。
但即使能更早、更準檢測出是否感染的核酸檢測試劑盒,其真實準確率也并不如人意。
據IVD從業者保守估計,目前獲得CE認證的核酸檢測試劑盒,其真實準確率平均只在70%左右,樂觀來看,也不過80%~90%。
“在目前疫情集中爆發和大規模檢測情形下,難以避免出現假陰、假陽的狀況。”真邁生物CEO顏欽評價道。
綜合來看,導致假陰、假陽的因素主要有兩點:
一是基因靶點的選用。與基因測序技術的全面掃描不同,核酸檢測通過抽取新冠病毒特有且穩定的基因序列靶點作為是否感染的依據。雖然CDC基于分子探針技術給出了一個建議“靶點”,各廠家也進行了改良和優化,但由于時間倉促,靶點的選用也未能經過充分驗證,因此客觀而言,產品設計確實不夠完善。
二是取樣和檢測。核酸檢測試劑盒的使用需要一線醫務人員進行取樣和設備實驗。其中,咽拭子是最主流的取樣方案,在這一過程中,取樣的部位和操作會影響到樣本新冠病毒數量的多少;同時,通過口腔提取樣本時可能會碰到牙齒,口水,樣本受到污染;此外,實驗人員在使用檢測試劑時,是否嚴格遵守了SOP(Standard Operating Procedure,標準作業程序)的標準操作規范,也會影響檢測結果。
除了難以在短期內突破準確度的天花板外,前段時間紛至沓來的訂單,也令臨時增開產線的IVD廠商手忙腳亂。
供應鏈公司在詢價過程中發現,不少已拿到CE認證的IVD企業并不能快速響應訂單需求。而要啃下量產的硬骨頭,最大的瓶頸不是人,而是設備和場地。
海普洛斯許明炎告訴「甲子光年」,核酸檢測試劑盒的生產流程跟機械化工廠中高度自動化的裝配流水線不同,需要專業的實驗人員在達到GMP標準(Good Manufacturing Practices,是一套適用于制藥、食品等行業的強制性標準,以確保最終產品質量符合法規要求)的生產車間里完成。
疫情導致的招工難雖沒有直接波及科研屬性較強的IVD行業,但裝修工人短缺,卻給實驗室擴建帶來了阻礙;此外,生產車間內原料、儀器設備的采購和布置需要較多的時間、人力和資金投入,實現量產的時間周期可能會很長。
因此,在工位比人力更金貴的情況下,臨時增開生產線的IVD廠商面臨著心有余而力不足的窘況——難以實現敏捷調度,只能通過輪班制擴大產能。
而商務部的限制條令發布后,可以預判,此次扎堆進來的小企業可能會經受較大損失。出海的訂單會向少數大企業聚攏,如華大基因、邁瑞醫療、萬孚生物等。
目前,國內企業中僅華大基因一家公司的IVD產品獲得了美國FDA認證。
在國內競爭之外,中國IVD廠商的共同對手則是跨國大型醫藥企業。
此前,全球IVD市場格局已呈現出高度集中的狀態。
五大巨頭企業羅氏、雅培、丹納赫、西門子和賽默飛在2012年到2017年的全球市場總占比穩定在57%左右,其中羅氏1家企業的市占率高達20%;中國IVD市場56%的份額也被這5大跨國巨頭占據,而國內最大的IVD企業邁瑞醫療僅占國內市場3.1%的份額。
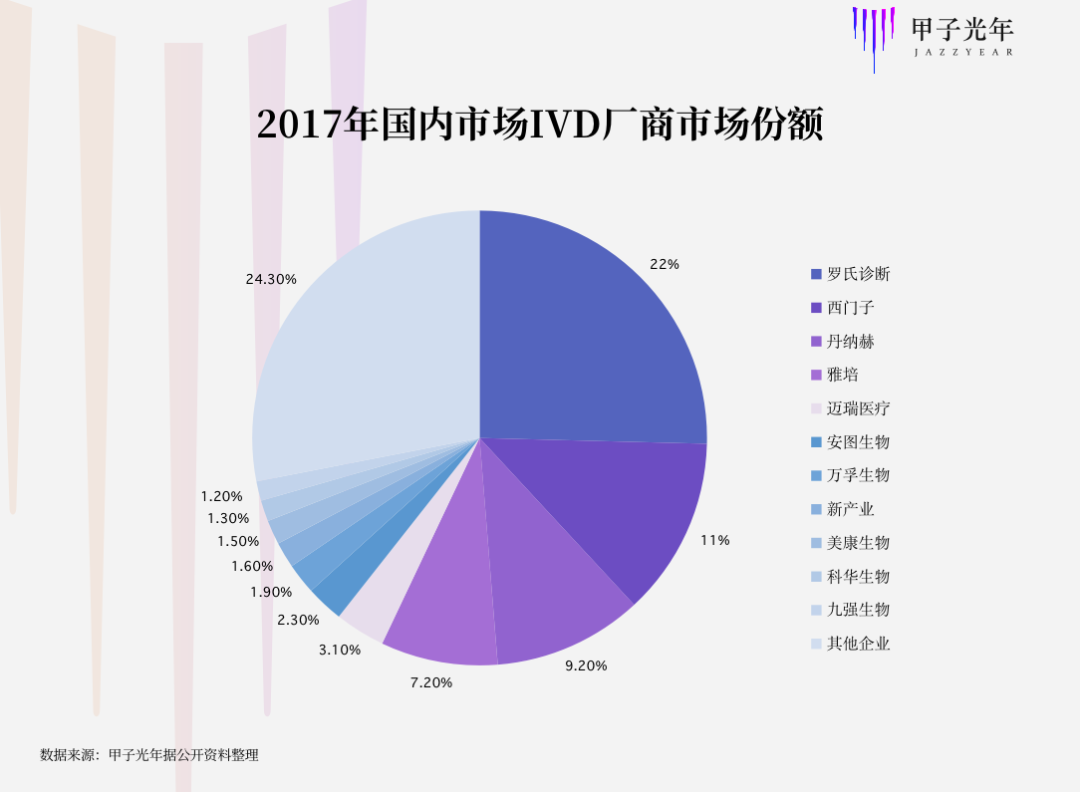
具體到新冠病毒上,由于疫情最先在中國爆發,國產IVD公司得以先行一步,但羅氏、雅培、丹納赫、西門子和賽默飛等國際巨頭也極有可能快速趕超——
3月25日,珀金埃爾默旗下的新冠病毒核酸檢測試劑盒獲得美國FDA批準緊急使用授權;3天后,雅培新冠病毒POCT檢測設備也通過了FDA的審批,雖然準確率有待驗證,但檢測速度驚人,據稱可在5分鐘內給出陽性結果,13分鐘內給出陰性結果。
這不僅反應出海外巨頭不容小覷的實力,也從側面說明出海熱是一時的,從技術本身而言,中國IVD行業的出海之路依然漫長。
綜合各種因素,中國IVD廠商想要搭上出海快車絕非易事。
許多業內人士并不認為此次疫情帶來的訂單潮會成為國內IVD企業國際化的最佳契機。
遠毅資本合伙人楊瑞榮告訴「甲子光年」,單憑一時的“訂單熱”并不能預測“出海潮”的到來,國產IVD企業的實力還遠不到與國外巨頭抗衡的水平。
3.材料、設備卡脖子
國內IVD企業的國際化程度確實較低。
以營收為例,海外業務占比超過10%已能領跑國內IVD企業的國際化水準。
即便是深耕IVD賽道多年的大型上市公司,其海外的銷售占比也極少超過20%——萬孚生物在2018年海外市場的銷售占比相對較高,為23.2%;三諾生物同年的海外市場占比為20.7%;華大基因緊隨其后為19.12%;博暉創新為15.9%;其他超過10%的國內企業還有艾德生物。
宏觀來看,IVD行業的全球市場和中國市場都呈現出“5+X”的相似格局。
羅氏、西門子、丹納赫、雅培、賽默飛占據了超50%的市場份額,而國內企業則呈現出“小而散”的市場狀況——僅10家企業在國內市場占比超1%。
其中,產業鏈上游的原材料,如電子元器件、診斷酶、抗原、抗體、精細化學品等對國外的進口依賴最強;中游的診斷試劑和診斷設備相對成熟,但市場競爭激烈,主要市場仍然被國際巨頭把持。
可見,中國IVD企業面臨的挑戰,不止“走出去”,還有“國產化替代”。
類比視之,IVD的行業生態與芯片頗為相似——關鍵原料/核心零部件的自研自產是實現國產替代的硬壁壘,而試劑配置/器件封裝則主要比拼渠道、市場和品牌之類的軟實力。
不少IVD從業者判斷,對原材料和設備的進口依賴或許會成為中國IVD行業的發展瓶頸。
先說材料,高端材料非常依賴進口,疫情期間更是有價無市。
以上游原料的酶工程[1]為例,雖然國內少數企業,如上海生工生物、菲鵬生物、阿匹斯生物、瀚海新酶等已能夠量產使用頻率較高且大眾化的酶產品,且性價比往往高于國際巨頭,但由于工藝導致的純度差異,國內許多IVD企業仍選擇直接采購國外的進口酶。
許明炎告訴「甲子光年」,酶的純度不僅會影響反應速率,甚至會影響到實驗的最終結果。尤其疫情突發的背景下,新冠病毒的抗體抗原在市場上實屬罕見,國內、國外的IVD上游試劑供應商并不能敏捷響應市場需求,一度陷入有價無市的窘況,并直接導致了免疫診斷法新冠病毒試劑盒在研發和生產周期上的滯后。
“核酸和膠體金法兩種檢測試劑盒的研發是同步啟動的,”許明炎補充道,但與已經通過CE認證的核酸檢測試劑盒相比,膠體金法的檢測試劑盒直到最近才研發完成,核心原因在于“前期根本買不到原料”。
抗疫期間真邁生物共免費捐贈了20萬人份的新冠病毒檢測試劑原料,這些原料都是自研自產的。真邁生物是一家專注于第三代基因測序技術的上游廠商,掌握酶、染料、堿基等IVD原料的關鍵核心技術。據CEO顏欽介紹,IVD原料是檢測試劑盒生產加工的核心,它的自主生產需要長期的技術積累,建立嚴謹的流程、工藝、管理體系,才能突破。目前這些關鍵技術大部分仍掌握在歐美公司手中,而目前國內的IVD原料生產廠商鳳毛麟角,還不能大規模滿足國內IVD的產業需求,這是整個行業的短板,急需攻克和補齊。
再說設備,核心零部件依賴進口,高端市場被海外公司把持。
整體來看,中低端市場實現國產替代易,而高端市場實現國產替代難。
類似PCR儀的大多數檢測設備,技術門檻并不高,邁瑞、貝瑞、美康、科華和安圖等企業其實在機電系統的設計制造及相關人才的培養監管層面已相當完善。
但基因測序儀、質譜儀、高效液相色譜儀、CT機、核磁共振儀等高端醫療器械或檢測設備,短期內仍無法實現國產替代。
以分子診斷中的基因測序儀為例,目前全球60%以上的市場都被Illumina和Oxford Nanopore Technology(ONT)壟斷,其中Illumina幾乎把持了國內三甲醫院的市場。
此外,基因測序儀往往需要配套同品牌的檢測試劑,而耗材是IVD上游企業的主要營收來源,這意味著設備國產化替代的渠道成本很高,會受到來自老巨頭和醫院雙方的阻力。
而目前國內自研的基因測序儀雖然實現了技術突破,但距離真正的商業落地還有一段距離。
2013年收購了美國上市公司Complete Genomics的華大基因,在2015年10月已推出了擁有完全自主知識產權的BGISEQ-500高通量桌面型基因測序儀。
但IVD從業者普遍認為,旗下產品并未完全成熟,在國內的市場化程度不高,跟國外相比還有一定差距。
真邁生物旗下的單分子測序系列產品已于2019年12月獲批歐盟CE標志,近半年來共收到1500萬元的銷售訂單,產品開始慢慢推向市場——采用定點投放、長期租賃以及與醫院課題組進行科研合作等方式進行國內推廣。
由于原料的質量直接決定體外診斷試劑的質量和穩定性,因此不得不依賴進口;即便已經在技術上實現了部分突破的中高端IVD儀器,從巨頭手中搶回市場也需要一定的時間。
總體而言,IVD行業的國產化替代依然充滿了機會和挑戰。
4.窗口期和洗牌期一起到來
中國的IVD市場雖然起步較晚,處于發展的早期階段,且原材料和高端設備等核心利潤環節仍被海外巨頭把持,但隨著老齡化、城鎮化、醫保支付能力增強、分級診療、保健意識增強等需求端因素的推動,以及技術進步、新項目臨床開展、原輔料升級等供給端能力的提升,中國已成為全球IVD行業增速最快的市場之一。
近年來,國內IVD行業已經涌現出了以達安、華大、邁瑞、萬孚、迪安、金域等為代表的標桿企業,尤其基因測序這個萬億市場更被視為彎道超車的主戰場,2010年前后,基因測序領域迎來了美吉生物、基準醫療、海普洛斯、真邁生物、銳翌生物等一波新秀。
從全行業來看,2012至2019年,中國IVD市場的年復合增速高達19.31%,遠高于同期全球市場8.20%的年復合增速。根據Frost & Sullivan數據,預計到2019年,中國IVD市場規模可達103.68億美元。
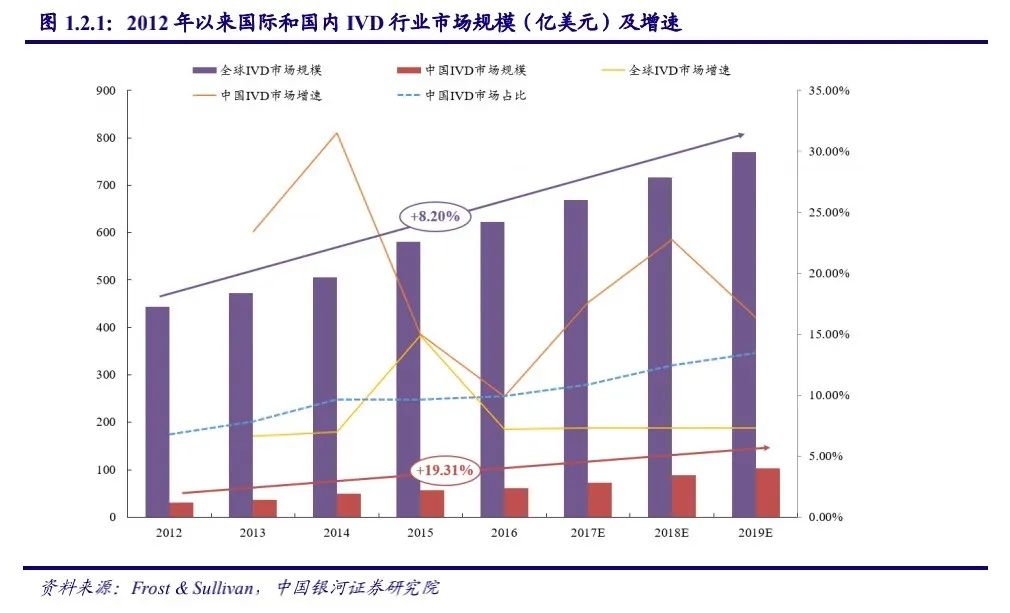
在中國體外診斷市場規模持續增長的同時,產品結構明顯改變。
生化診斷在細分領域市場占比由2012年的26%下降到19%,而免疫診斷、分子診斷和POCT(point-of-care test,即時檢測)近年市場占比顯著提升。
·目前,已有超200家國內企業入局生化診斷領域,生化診斷市場的國產試劑占有率已超過50%,創業的空間較小;
·免疫診斷是我國近年IVD領域增速最快的賽道之一,增速達15%以上,其中化學發光占比約75%;
·至于分子診斷,我國雖然起步晚但起點高,我國熒光定量PCR技術已達到國際先進水平,基因芯片和基因檢測接近國際水平。
遠毅資本楊瑞榮告訴「甲子光年」,雖然國際巨頭在中國IVD市場占據主導地位的狀況會持續一段時間,但低、中、高三條細分市場的國產化替代進度卻不同:
·較低端的早孕POCT、血糖儀、血糖試紙等“低科技”設備,已開始大量出口海外;
·中端的化學發光產品正處在國產化替代的緩慢進程中,可能需要5~10年才會完成;
·而結合AI大數據和生物信息學研究成果的精準診療,包括基因測序和質譜分析等相關產品,在未來的3~5年,有很大的機會可以彎道超車。
其次,在基因測序領域,中國還有一個天然優勢,即巨大人口規模形成的天然樣本庫。
由于儀器檢測的準確性與機器學習原理類似,樣本量越大越能在實踐中建立更完善的大數據模型,更有可能形成算法優勢,研發出新的應用,提升檢測能力和水平。以目前基因測序技術在腫瘤領域的應用來看,其樣本量和檢測準確度已經超越了測序儀的主要出口國。
“在癌癥個性化的應用上,中國的基因測序企業已經走向世界了,”楊瑞榮補充道,2019年末,華大智造的測序儀參與“阿布扎比全民基因組計劃”,為阿聯酋全民提供基因測序技術和平臺服務,就是一個標志性事件。專注于在基因測序平臺做液體活檢癌癥早篩的基準醫療也已經開始和某跨國藥企在全球的技術合作。
而掌握了原料關鍵技術的真邁生物,已開發出了適用于第二代測序儀的建庫試劑盒,或將由于國內的巨大需求拿下數十萬級檢測量的長期生意,“中國每年大概有2000萬例基因測序樣本,每一例上機測序都需要進行建庫,成本從幾十元到一百多元不等,”真邁生物CEO顏欽稱,旗下產品已在美吉生物、圣湘生物和達瑞生物的平臺上完成了測試,“如果能夠通過控制成本,搶到這一塊存量市場,也是非常不錯的收入。”
具體到各細分市場,中國的基因測序賽道還有以下切入點:
1)試管嬰兒
目前中國的不孕不育率高達25%,以去年1300萬新生兒的數量為標準,每年有300多萬家庭無法生育;其次,目標人群對高客單價的接受度較好,這一市場的潛在容量極大,且由于樣本有限,在技術層面有較大的限制和壁壘,很容易搭建護城河。
2)腫瘤癌癥
國內腫瘤賽道的早期公司,已在肺癌、腸癌、肝癌、乳腺癌等大癌腫的基因篩查領域積累了2~3年的行業經驗,創業機會相對較少;但還有些比較冷門的小癌腫尚未被覆蓋,例如前列腺癌、食管癌等,可作為市場切入點,建立品牌,擴大業務范圍。
3)遺傳病
據統計,由于基因突變引起的人類遺傳病超過7000種,目前能夠確診的遺傳病僅2000種左右。如何避免單基因遺傳性疾病,做好優生優育,目前這個市場還有非常大的潛力,如果有特別看好的創業者可以入局。
4)病原微生物
多用于ICU快檢的病原微生物檢測,也是近兩年比較火熱的賽道。例如,2020年2月以來,專注于微生物細分賽道的慕恩生物、予果生物就分別披露了近億元及數千萬人民幣的巨額融資。
目前看來,中國IVD行業似乎是一座高毛利、多切口的創業金礦,但“帶量采購”——由國家組織的藥品集中采購,一般價格會更低——一直是懸在所有企業頭頂的一把達摩克利斯之劍。
由于IVD行業生態“雜”而“散”,從B端廠商到C端消費者的產業鏈很長,細分領域中的競爭較小,因此國內IVD企業的日子還算愜意。
但不少從業者觀察,根據前期仿制藥實行“帶量采購”的經驗來看,該項政策一旦推進,銷售的中間成本被省去,IVD行業毛利率可能會驟降到20%~30%,行業會進入長期的并購、重組階段,格局未定的賽道將迎來新一輪的洗牌。
IVD產業雨露均沾的混沌階段恐怕要到頭了,出海潮連著退貨潮,最后的局面還是贏家通吃。
[1]酶工程又稱蛋白質工程學,是指工業上有目的的設置一定的反應器和反應條件,利用酶的催化功能,在一定條件下催化化學反應,生產人類需要的產品或服務于其它目的的一門應用技術。
?2020年Q1投資報告:僅634起投資,同比下降44.5%;生物制藥受疫情利好顯著 | IT桔子報告
?連續投資 3 次或更多,那些被 IDG 重注的公司現在發展如何??從頭開始捋:騰訊是如何做投資的??疫情中發揮重要作用的「宏基因組測序」,在本季度獲得資本追捧?一邊升級支付寶,一邊投資布局,阿里巴巴的「本地生活」進階史?逆風而上,「高紅騰」資本三雄 加足馬力投資掃貨?2019-2020 年消費升級影響下的新商業模式研究丨IT桔子報告
?向死而生,比金子更寶貴的是信心!《2019-2020 年新經濟創業投資盤點》發布


